阅读:0
听报道
2019年7月4日,正大天晴为其ALK抑制剂TQ-B3139胶囊登记了一项新的Ⅲ期临床试验,试验登记号是NCT04009317,试验标题是《Study of TQ-B3139 Versus Crizotinib in the First Line Treatment of Subjects With Anaplastic Lymphoma Kinase (ALK) Positive Non-Small Cell Lung Cancer (NSCLC)》,可译为“TQ-B3139对比克唑替尼一线治疗ALK阳性的非小细胞肺癌的临床研究”,目前尚未开始招募患者。不过,这一临床试验的登记证明,TQ-B3139胶囊已进入Ⅲ期临床试验。
TQ-B3139的受理号是CXHL1501760(原料药)、CXHL1501759(制剂),申请的企业是“连云港润众制药有限公司、正大天晴药业集团股份有限公司、北京赛林泰医药技术有限公司”,于2015年8月4日申请临床,2016年5月23日获批临床。
在最新的这个Ⅲ期临床试验之前,该新药曾有一个Ⅰ期临床试验,登记号是CTR20170398,首次公示信息日期是2017年4月24日,第一批受试者入组日期是2017年7月18日。该试验目前的状态仍是“进行中(招募中)”,而实际上可能已完成,但公司没有更新该临床试验的登记信息。我们也没有搜索到关于该新药的临床数据。
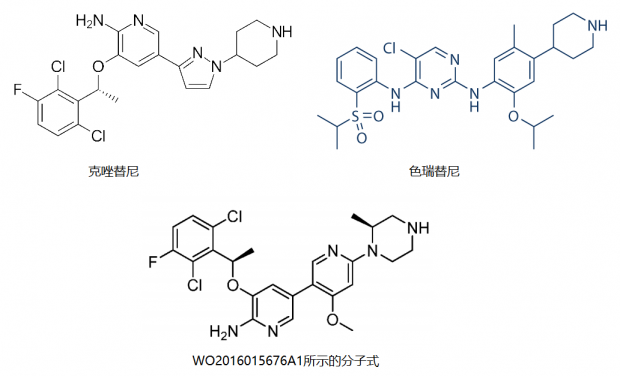
通过对专利数据库的搜索,我们发现一份专利可能是该新药的化合物专利,专利号为WO2016015676A1,名称为《吡啶取代的2-氨基吡啶类蛋白激酶抑制剂》,申请人为正大天晴药业集团股份有限公司、连云港润众制药有限公司、北京赛林泰医药技术有限公司。由此,我们可以对比专利中所示的分子式与第一代ALK抑制剂克唑替尼和第二代ALK抑制剂色瑞替尼的分子式,如下图所示:
目前,国内已经上市了两个第二代ALK抑制剂,即诺华的色瑞替尼(Ceritinib)和罗氏的阿来替尼(Alectinib),国内药企贝达药业的第二代ALK抑制剂恩莎替尼预计也会在不远的将来上市,而国外,第三代ALK抑制剂,辉瑞的劳拉替尼(Lorlatinib),也已于2018年11月获得FDA批准上市。
国内外ALK抑制剂的进展反而使这个Ⅲ期临床试验显得令人困惑。主要有:
一是在这个Ⅲ期临床试验中,使用的对照药是第一代ALK抑制剂克唑替尼。即便该新药成功击败克唑替尼,但也仅证明它是第一代ALK抑制剂的me-better,而无法证明它是第二代甚至第三代ALK抑制剂的me-better;
二是由于采用第一代ALK抑制剂克唑替尼作为对照药,而患者可能更愿意使用第二代ALK抑制剂治疗,因此这个Ⅲ期临床试验可能遇到招募患者方面的困难;
三是根据该临床试验的登记信息,该研究的预计完成时间是2022年4月30日,考虑到数据分析、申报审批等工作需要大量的时间,即便这些流程顺利,该新药获批上市的时间可能是2023或2024年。而第一代ALK抑制剂克唑替尼在国内的化合物专利将于2024年到期;第二代ALK抑制剂色瑞替尼甚至在国内没有化合物专利,仅获得了适应症专利,结构通式专利也还在实质审查阶段,总体看专利保护较弱。因此,如果该新药有机会上市,那么在上市之时可能面临非常激烈的竞争;
四是患者群体较小。有数据显示,国内肺癌每年新发病患者数量超过73万人,其中58.4万人是非小细胞肺癌,而仅有约3.5万人为ALK阳性。由于不同的数据源的数据不一致,因此估计每年新发病的ALK阳性非小细胞肺癌的患者数量在3~7万人之间。这并非一个较大的数字,而其中参与竞争的企业较多。因此,此前启动研发费用较高的Ⅲ期临床试验,未来是否能顺利收回投资?
正因为存在上述疑问,该公司在当前时点启动Ⅲ期临床试验就显得令人困惑。如果有谁了解相关情况,欢迎评论或私信,谢谢!
话题:
0
推荐
财新博客版权声明:财新博客所发布文章及图片之版权属博主本人及/或相关权利人所有,未经博主及/或相关权利人单独授权,任何网站、平面媒体不得予以转载。财新网对相关媒体的网站信息内容转载授权并不包括财新博客的文章及图片。博客文章均为作者个人观点,不代表财新网的立场和观点。




 京公网安备 11010502034662号
京公网安备 11010502034662号 